Cookie Settings
当社は、お客様に最適な体験を提供するためにクッキーを使用しています。 技術的に必要なクッキーはショッピングを可能にするために使用され、統計は匿名化されたGoogleアナリティクスに使用されます。 すべては、更新された プライバシーポリシー.
| サンプル材料 | 50ml EDTA全血 |
| 断熱方法 | 300μl CD19 S-pluriBeads®抗ヒトを使用した非磁性体 |
| 収量 | ~3.5 * 10^6 Bリンパ球 |
| バイタリティ | >99% (トリパンブルーの染み) |
| 純度判定 | 抗CD20 FITC抗体染色後、FACS分析。 |
| 純度 | ~97% Bリンパ球 |
標的活性化後、抗体分泌性血漿細胞(ASC)の豊富さをELISpotで測定した。
単離したB細胞をポリクローナル活性化混合物で5日間刺激した。次いで、それらを特異的抗原でコーティングしたプレート上で増殖させた。24時間のインキュベーション後、アッセイを行った。
得られたスポットを専用ソフト(AID ELISpot6.0 iSpot)を用いて計数し、評価した。隣接する図において、青色の数字はウェルあたりの抗原特異的スポットの数を示している。
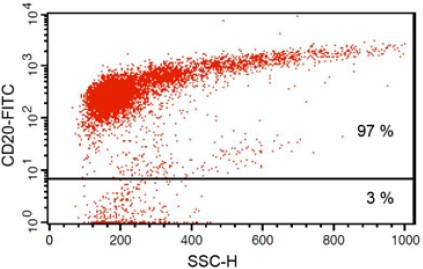
Fig 1: 単離・刺激されたBリンパ球の純度
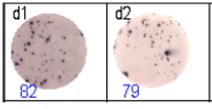
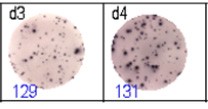
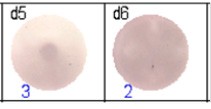
Fig 2: 重複して抗Ig特異的細胞のELISpot分析を行った。 d1d2:250細胞/ウェルずつ、d3d4:500細胞/ウェルずつ、d5d6:非活性化細胞(500細胞/ウェルずつ)
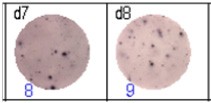
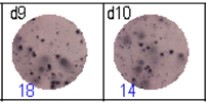
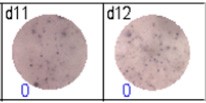
Fig 3: d7d8: 抗インフルエンザヌクレオカプシド特異的メモリーB細胞、d9d10:NTI破傷風トキソイド特異的メモリーB細胞、d11d12:ネガティブコントロール
S-pluriBead® CD19は、ヒト全血サンプルからBリンパ球を97%の純度で分離することを可能にしました。
単離されたターゲットは、トリパンブルー染色後に99%以上の生存率を示した。これらは、細胞培養での増殖に成功し、抗体分泌プラズマ細胞(ASC)へと分化した。ASCsはELISpotアッセイによる抗原特異的メモリーB細胞応答の解析に適していることがわかった。結果は、参照法(Dynabeads® CD19 Pan B)で得られた結果と同等であった。
参照方法については、出版物を参照してください: Bussmann BM, Reiche S, Bieniek B, Krznaric I, Ackermann F, Jassoy C: Loss of HIV-specific memory B-cells as a potential mechanism for the dysfunction of he humoral immune response against HIV. Virology 2010; 397(1):7-13.)